Контакти:Еррол Чжоу (містер)
тел.: плюс 86-551-65523315
Мобільний/WhatsApp: плюс 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Електронна пошта:sales@homesunshinepharma.com
додати:1002, Хуаньмао Будівля, №105, Менчен Дорога, Хефей Місто, 230061, Китай
Нещодавно відкрита мітка II націленого протипухлинного препарату AstraZeneca (Коселуго) (селуметиніб) для лікування симптоматичної, нерезектабельної плексиформної нейрофіброми (ПН) у педіатричних пацієнтів з нейрофіброматозом типу 1 (NF 1). SPRINT Stratum 1 випробування (NCT0 1 362803) були опубліковані в Інтернеті в New England Journal of Medicine (NEJM). Заголовок статті: Селуметиніб у дітей з неоперабельною плексиформною нейрофібромою.
NF 1 - генетичне захворювання нервової системи, яке спричинює зростання пухлин на нервах. Ці пухлини (плексиформна нейрофіброма) можуть рости в будь-якому місці тіла, включаючи обличчя, кінцівки, навколо хребта та ділянки тіла, які можуть вражати органи. Найпоширеніші симптоми, пов'язані з нейрофіброматозом, включають знебарвлення, рухову дисфункцію та біль. Дані дослідження SPRINT Stratum 1 показують, що лікування Koselugo має значні клінічні переваги для пацієнтів, які можуть продовжувати зменшувати об'єм пухлини, полегшувати біль, покращувати щоденні функції та загальну якість життя, пов’язану зі здоров’ям.
Koselugo - це новий інгібітор пероральної кінази, який був затверджений FDA США в середині квітня цього року. Застосовується для педіатричних пацієнтів з нейрофіброматозом типу {{{1}} (NF 1) у віці 2 років і старше для лікування НФ 1, пов'язаного із симптоматичним та неоперабельним плексичним нейрофіброматозом. (PN). Варто згадати, що Коселуго - це перший препарат, схвалений FDA США для лікування НФ 1. Раніше Коселуго було присвоєно кваліфікацію до наркотиків-сиріт (ODD) та проривну кваліфікацію щодо наркотиків (BTD) за лікування НФ 1. Коселуго є інгібітором кінази, тобто він діє через ключові ферменти, запобігаючи тим самим ріст пухлинних клітин.
Плексусна нейрофіброма (ПН) (Джерело зображення: Canceworld.info)
NF 1 - рідкісне захворювання, яке виснажує, прогресує і часто викликає викривлення. Це захворювання, як правило, починається на початку життя і викликається мутаціями або дефектами конкретних генів. NF 1 зазвичай діагностується в ранньому віці. NF 1 зустрічається приблизно у кожного з 3, 000 немовлят і характеризується зміною кольору шкіри (пігментація), ураженням нервів та кісток та ризиком розвитку доброякісних та злоякісних пухлин протягом життя. {{ 3}} 0% до 50% пацієнтів з НФ 1 мають одну або кілька плексиформних нейрофібром (ПН). Основним методом лікування ПН є хірургічна резекція. На жаль, через розташування або об’єм цих пухлин багато пацієнтів не підходять до операції. Крім того, НП зазвичай рецидивує після оптимальної хірургічної резекції і тому є важливою сферою, де медичні потреби не задовольняються.
Програма SPRINT Stratum 1 була спонсорована Національною програмою оцінювання ракової терапії Національним інститутом раку (NCI) (CTI). До випробування зараховано 50 педіатричних пацієнтів (середній вік 10. 2 років, діапазон: {{4}}. 5-17. 4). Ці діти мали NF 1 і не працюючий PN (визначається як PN, який неможливо повністю видалити, але не становить серйозної небезпеки для пацієнта). Найпоширенішими симптомами, пов’язаними з нейрофіброматозом, є знебарвлення (4 4 випадки), рухова дисфункція (33 випадки) та біль (26 випадки). Під час випробування пацієнти приймали Коселуго 25 мг / м 2 (затверджена рекомендована доза) двічі на день, поки стан не погіршився або не виникли неприйнятні побічні реакції. Під час випробувального періоду регулярно оцінювали зміни обсягу пухлини у пацієнта 0010010 # 39; симптоми захворювання, пов'язані з пухлиною, і визначали загальну швидкість відповіді (ORR), яку визначали як: { {4}} - 6 місяців методом МРТ підтвердили повну або часткову ремісію (зменшення об’єму пухлини PN ≥ 20%).
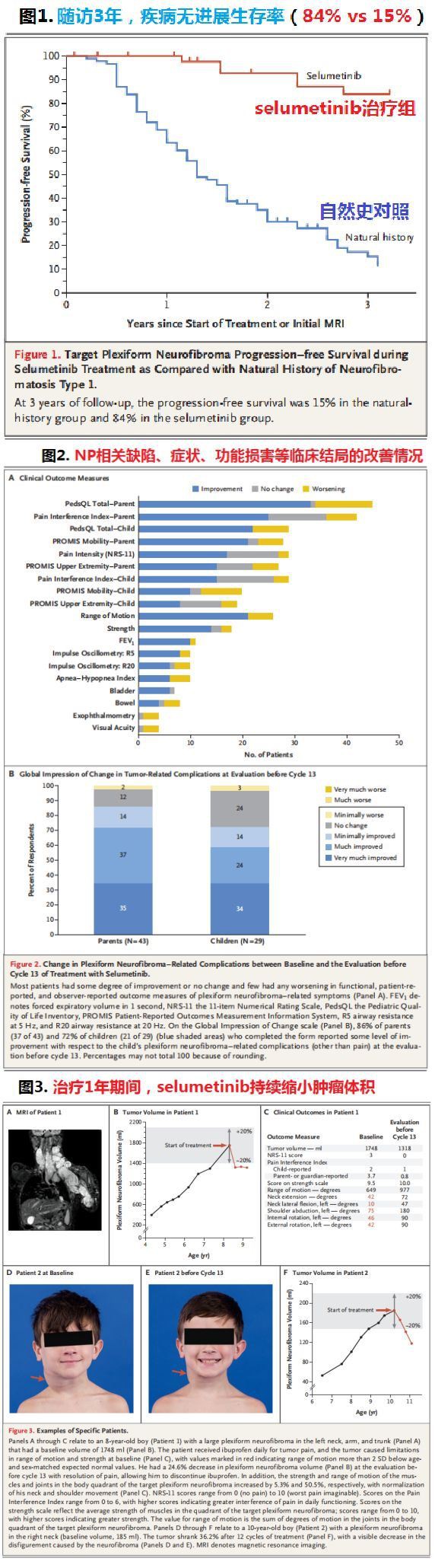
Дані, опубліковані в NEJM, показують, що станом на березень 29, 2019, 35 від 50 пацієнтів було підтверджено ремісію, тобто загальна швидкість ремісії (ORR) Коселуго вдвічі щоденна пероральна монотерапія становила 70% (n= 35 / 50), у всіх пацієнтів спостерігається часткова ремісія (PR). З 35 пацієнтів з підтвердженою ремісією, 28 (80%) виявив стійку ремісію (тривалість ремісії ≥ 1 рік). На додачу,
Випробування також оцінювало вплив Koselugo на інші клінічні результати, включаючи зміни ПН, пов'язані з дефектами, симптомами та функціональними порушеннями. Незважаючи на невеликий розмір вибірки пацієнтів, які оцінювали кожну захворюваність на ПН (такі як дефекти, біль, проблеми з силою та рухливістю, стиснення дихальних шляхів, порушення зору та дисфункція сечового міхура або кишечника), пов'язані з ПН недоліки, симптоми та функції під час лікування пошкодження також показали поліпшення.
Зокрема: після 1 року лікування показник інтенсивності больових відчуттів у пацієнта зменшився в середньому на 2 бали, що вважається клінічно значним покращенням. Крім того, щоденні функції (38% та 50% відповідно) та загальна якість життя (48% та 58% відповідно) та сила (56%) та діапазон руху (38%) у дитячих звітах та звітах батьків У результаті також спостерігалось покращення клінічної значущості.
Після трирічного спостереження рівень виживання захворювання без прогресування в групі лікування Коселуго становив 84%, порівняно з 15% у контрольній групі з історії історії. Під час випробування 5 пацієнти припинили лікування через можливі токсичні ефекти, пов’язані з Коселуго, а 6 пацієнти погіршилися. Найбільш поширені токсичні реакції - нудота, блювота, діарея, безсимптомне підвищення рівня креатинфосфокінази, вугроподібні висипання, пароніхія.
Діючим фармацевтичним інгредієнтом Коселуго 0010010 # 39 є селуметиніб, який є пероральним, сильним і селективним МЕК 1 / 2 інгібітором кінази. Ген NF 1 кодує нейрофібромін (нейрофібромін), який негативно регулює шлях RAS / MAPK і допомагає контролювати ріст, диференціювання та виживання клітин. Мутації гена NF 1 можуть спричинити нерегульованість сигнального шляху RAS / RAF / MEK / ERK, що може змусити клітини рости, ділитися та розмножуватися безконтрольно, а також може спричиняти ріст пухлини. Селуметиніб потенційно інгібує ріст пухлини, інгібуючи фермент МЕК на цьому шляху. В даний час селуметиніб оцінюється в клінічних дослідженнях як монотерапія та в поєднанні з іншими методами лікування декількох типів пухлин.
Array BioPharma відкрив селуметиніб, і AstraZeneca отримав дозвіл 2003 на отримання виключних глобальних прав на сполуку. У липні 2018 АстраЗенека та Мерк досягли стратегічного співробітництва в галузі онкології для спільної розробки та комерціалізації селуметинібу та інгібітора PARP Lynparza в усьому світі. В даний час обидві сторони проводять клінічне дослідження фази I / II, SPRINT, щоб вивчити потенційні переваги селуметинібу у педіатричних пацієнтів з неоперабельними плексиформними нейрофібромами, пов'язаними з NF1 (PN).
Нейрофіброматоз типу 1 (NF 1) є невиліковним генетичним захворюванням із захворюваністю від 3, 000 до 4, 000 у немовлят. Хвороба викликається спонтанною або генетичною мутацією гена NF 1 і пов'язана з багатьма симптомами, включаючи м'які скупчення (підшкірні нейрофіброми) на поверхні шкіри та шкіри, пігментацію шкіри (кавові молочні бляшки) , при доброякісних пухлинах оболонки нервових оболонок (плексиформні нейрофіброми [PN]) також можуть бути спричинені у 20% -50% пацієнтів. Ці плексиформні нейрофіброми (ПН) можуть спричинити біль, рухову дисфункцію та знесилення.
Люди з НФ 1 можуть зазнати багатьох інших ускладнень, таких як труднощі з навчанням, скручування та згинання хребта, гіпертонія та епілепсія. NF 1 також збільшує ризик для людини 0010010 # 39; інших захворювань на рак, включаючи злоякісні пухлини оболонки мозку та периферичного нерва та лейкемію. Симптоми захворювання починаються в ранньому дитинстві і сильно різняться за ступенем вираженості, що може скоротити тривалість життя на цілі 15 роки.
джерело:Селуметиніб у дітей з неоперабельною плексиформною нейрофібромою