Контакти:Еррол Чжоу (містер)
тел.: плюс 86-551-65523315
Мобільний/WhatsApp: плюс 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Електронна пошта:sales@homesunshinepharma.com
додати:1002, Хуаньмао Будівля, №105, Менчен Дорога, Хефей Місто, 230061, Китай
Онкологічна компанія Taiho Oncology під керівництвом японської фармацевтичної компанії Taiho Pharmaceutical нещодавно оголосила про ковалентно комбінований інгібітор FGFR футібатініб (TAS-120) Фаза 2 дослідження FOENIX-CCA2 на засіданні Американської асоціації з дослідження раку (AACR) 2021. Дані щодо ефективності та безпеки. Це багатоцентрове дослідження з однією групою, яке оцінює футібатиніб для лікування пацієнтів з локально запущеною або метастатичною внутрішньопечінковою холангіокарциномою (внутрішньопечінкова холангіокарцинома, iCCA), які мають перегрупування гена FGFR2 (включаючи злиття генів) і які отримали принаймні одне відмова від лікування. .
У ході випробування 103 пацієнти з перестановкою гена FGFR2 (включаючи злиття генів), які раніше отримували одну або кілька системних методів лікування, локально прогресуючі або метастатичні нерезектабельні пацієнти iCCA, отримували дозу 20 мг футибатинібу один раз на день до прогресування захворювання або неприйнятної токсичності.
Результати показали, що дослідження досягло первинної кінцевої точки об'єктивної реакції (ORR)> 20%, визначені незалежним оглядом та оцінкою центру: ORR футибатинібу становив 41,7%. Що стосується вторинних кінцевих точок, то ремісія була тривалою, із середньою тривалістю ремісії (DOR) 9,7 місяців, 72% ремісій ≥ 6 місяців та частотою контролю захворювань (DCR) 82,5%. Медіана виживання без прогресування (PFS) становила 9,0 місяців, медіана загальної виживаності (OS) становила 21,7 місяця, а 72% пацієнтів виживали через 12 місяців.
З точки зору безпеки, загальними побічними явищами, пов’язаними з лікуванням (TRAE), є гіперфосфатемія (85%), випадання волосся (33%) та сухість у роті (30%). Найпоширенішим TRAE 3 ступеня є гіперфосфатемія (30%), яка зникає після належного лікування. Повідомлялося про випадки підвищеного рівня трансаміназ 4 ступеня та не повідомлялося про смерть, пов’язану з лікуванням.
Ліпіка Гоял, доктор медичних наук, провідний дослідник дослідження та онколог онкологічного центру Массачусетської загальної лікарні, сказала:" Результати дослідження FOENIX-CCA2 мають велике значення для пацієнтів з рефрактерною внутрішньопечінковою холангіокарциномою із злиттям гена FGFR2 або інші перестановки. Оскільки футибатиніб продемонстрував значущу терапевтичну ремісію, ORR становив 41,7%, а стійкість ремісії була хорошою. Ці результати представляють ще один приклад обіцянки прецизійної медицини від холангіокарциноми та вказують на те, що у разі схвалення футібатиніб може надати нове рішення для пацієнтів з рефрактерними варіантами лікування CCA."
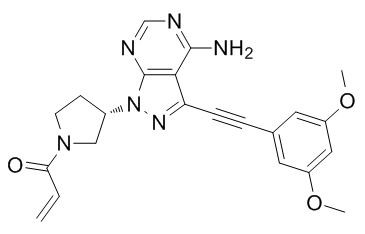
Молекулярна структура футібатинібу (TAS-120) (джерело зображення: macklin.cn)
У лютому 2021 року, на основі даних дослідження FOENIX-CCA2, FDA США надала проривне призначення препарату футібатініб (BTD) для лікування місцево просунутих або метастатичних пацієнтів із перестановкою генів FGFR2 (включаючи злиття генів) і раніше пролікованих холангіокарциномою ( CCA) пацієнтів. У 2018 році FDA також призначила призначення препарату-сироти (ODD) для футибатинібу для лікування CCA.
Футібатініб (TAS-120) є недостатньо дослідженим, пероральним, сильнодіючим, селективним та незворотним інгібітором малих молекул FGFR1, 2, 3 та 4. В даний час він розробляється як лікування передових солідних пухлин з аномальними генами FGFR1-4. Потенційне лікування пацієнтів (включаючи холангіокарциному). У пухлинах, що несуть аберації гена FGFR1-4, футибатиніб може селективно і незворотно зв'язуватися з кишенею зв'язування АТФ FGFR1-4, що призводить до інгібування опосередкованих FGFR шляхів передачі сигналу, зменшення проліферації пухлинних клітин та загибелі пухлинних клітин. .
Мартін Дж. Біркхофер, доктор медичних наук, старший віце-президент та головний медичний директор онкології Taiho, сказав: «Оскільки рівень виживання пацієнтів з внутрішньопечінковою холангіокарциномою (iCCA), як правило, низький, безпечні та ефективні нові варіанти лікування є головним досягненням. Ми з нетерпінням чекаємо цього. Поділіться цими даними з контролюючими органами для підтвердження схвалення цього важливого терапевтичного препарату."
Холангіокарцинома (CCA) - це рак, який виникає в жовчних протоках і може бути класифікований за анатомічним походженням: внутрішньопечінкова холангіокарцинома (iCCA) виникає у внутрішньопечінковій жовчній протоці, а позапечінкова холангіокарцинома (eCCA) - у позапечінковій жовчній протоці. . Хворі на ТКА зазвичай перебувають на пізній або пізній стадії поганого прогнозу, коли їм ставлять діагноз. Захворюваність на CCA різниться залежно від регіону, а захворюваність у Північній Америці та Європі становить 0,3-3,4 / 100 000. П'ятирічна виживаність iCCA (усі стадії SEER складаються разом) становить 9%.
Основним методом лікування ККА є хірургічна резекція. Якщо пухлина не може бути повністю видалена хірургічним шляхом, а на краю тканини, видаленому хірургічним шляхом, виявляються ракові клітини (їх також називають позитивними краями), можуть застосовуватися променева терапія та хіміотерапія. Ані 3, ані 4 стадія раку неможливо повністю видалити хірургічним шляхом. В даний час стандартні варіанти лікування обмежені променевою терапією, паліативною допомогою, трансплантацією печінки, хірургічним втручанням, хіміотерапією та інтервенційною рентгенологією.
Рецептор фактора росту фібробластів (FGFR) відіграє важливу роль у проліферації, виживаності, міграції та ангіогенезі пухлинних клітин (утворенні нових судин). Злиття, перебудова, транслокація та ампліфікація генів у FGFR тісно пов'язані з появою та розвитком різноманітних пухлин. Злиття або перебудова FGFR2 відбувається майже виключно при iCCA і спостерігається у 10-16% пацієнтів.

Пемазир-пемігатиніб (інгібітор FGFR, джерело зображення: medchemexpress.cn)
Що стосується цілеспрямованої терапії CCA, препарат Пемазир, розроблений біологічним партнером Cinda' біологічним партнером Incyte, був схвалений США, Європейським Союзом та Японією відповідно для лікування раніше отриманого лікування, Злиття або рецидив FGFR2 Пацієнти з локально запущеною або метастатичною холангіокарциномою, яких неможливо видалити хірургічним шляхом.
Варто згадати, що Пемазир - перша та єдина цілеспрямована терапія холангіокарциноми у США, Японії та Європейському Союзі. Препарат може блокувати ріст і поширення пухлинних клітин, блокуючи FGFR2 в пухлинних клітинах. Оскільки холангіокарцинома є руйнівним раком із серйозними незадоволеними медичними потребами, Пемазир раніше отримував статус наркотиків-сирот, статус проривного препарату, статус пріоритетного огляду та прискорену оцінку.
Активний фармацевтичний інгредієнт пемазире&# 39 пемігатиніб є потужним, селективним пероральним інгібітором малих молекул проти ізомерів 1, 2 та 3 FGFR. У доклінічних дослідженнях було підтверджено, що пемігатиніб має потужну та селективну фармакологічну активність щодо ракових клітин з FGFR генні зміни.
Нормативні затвердження Pemazyre' США, Японії та Європейського Союзу базуються на даних, заснованих на дослідженні FIGHT-202. Дослідження проводили у пацієнтів з місцево-поширеною або метастатичною холангіокарциномою, які раніше лікувались для оцінки ефективності та безпеки Пемазиру. Результати дослідження нещодавно були оголошені на конференції Європейського товариства медичної онкології (ESMO) 2019. Дані показують, що серед пацієнтів із злиттям або перебудовою FGFR2 (когорта A), медіана спостереження 15 місяців, загальна кількість монотерапії Пемазиром Частота відповіді (ORR) становила 36% (первинна кінцева точка), а медіана тривалості відповідь (DoR) становив 7,49 місяців (вторинна кінцева точка).
У грудні 2018 року Cinda Biotech досягла стратегічної співпраці та ексклюзивної ліцензійної угоди з Incyte щодо сприяння клінічній розробці трьох лікарських засобів (ітацитиніб, парсаклізіб, пемігатиніб) при одноразовій або комбінованій терапії в материковому Китаї, Гонконгу, Макао та Тайвані. І комерціалізація. Згідно з умовами угоди про співпрацю, Incyte отримає від Cinda Bio перший внесок у розмірі 40 мільйонів доларів США, а також другий готівковий внесок у розмірі 20 мільйонів доларів США після першого подання нової заявки на ліки в Китаї в 2019 році. Крім того, Incyte матиме право на виплати потенційних етапів розвитку до 129 мільйонів доларів США та потенційні комерційні виплати до 202,5 мільйонів доларів США.